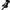Ova slika sa crvenim zeljem budi sjetne uspomene na prvi sat kemije u 7. OŠ i na pomalo nespretnog ali entuzijastičnog nastavnika kemije. 
Kemičar u kući (#51): O čemu ovisi boja hrane

- poruka: 3
- |
- čitano: 10.034
- |
- moderatori:
vincimus
- +/- sve poruke
- ravni prikaz
- starije poruke gore
Zanimljiv članak!
U kontekstu boja i kiselosti, čime se i koliko kiseli da dobija svaku drugu boju?!
 ATJ Lučko
ATJ Lučko
Može se kiseliti bilo čime, octenom, liumnskom, solnom ili sumpornom kiselinom. Boja ovisi o pH, a pH je negativni logaritam koncentracije vodikovih iona, pH = -log [H+], drugim riječima koncentracija vodikovih iona na logaritamskoj skali. Stoga je za boju indikatora potpuno svejedno od koje kiseline ti ioni dolazili. Nijansa boje ovisi pak o pH no na dosta složen način, jer se svi oblici indikatora nalaze u ravnoteži, koja opet ovisi o koncentraciji pH iona. Stoga ni pri jednoj pH-vrijednosti nemamo samo jednu formu indikatora, no kad koncentracija jedne forme prevagne, indikator će poprimiti njegovu boju.
Sve se to može izraziti jednadžbom:
-log K = log[HL]/[L] - pH
gdje je K konstanta ravnoteže (ona se utvrđuje eksperimentano), [HL] koncentracije "kisele" forme indikatora, a [L] koncentracija bazne forme indikatora. Omjer koncentracije dviju boja, [HL]/[L], bit će očito (kad se navedena jednadžba malo pretumba):
log [HL]/[L] = pH - log K
iz čega se vidi ovisnost o pH. Još treba reći sa za svaki oblik indikatora može napisati takva jednadžba, s različitim vijednostima konstante K. Mislim da je sada stvar malo jasnija.